Młodzi naukowcy z Centrum Badawczo-Rozwojowego American Heart of Poland (CBR AHP) z sukcesem dokonali implantacji pierwszych prototypów pierwszego polskiego całkowicie biodegradowalnego stentu do tętnic wieńcowych świni.
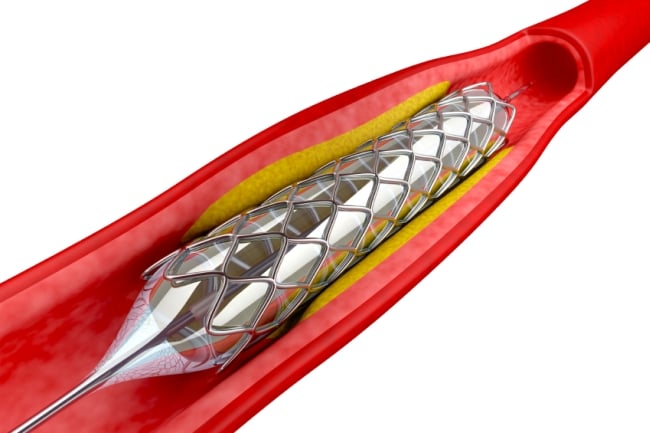
Projekt pod nazwą „Apollo” realizowany jest w ramach grantu z Narodowego Centrum Badań i Rozwoju „Strategmed” przez konsorcjum podmiotów, których liderem jest CBR AHP a współwykonawcami polska firma Balton, Centrum Materiałów Polimerowych i Węglowych PAN, Wydział Inżynierii Biomedycznej Politechniki Śląskiej, Śląskie Centrum Chorób Serca w Zabrzu, Wydział Mechaniczny Wojskowej Akademii Technicznej oraz firma Innovations for Heart and Vessels.
Głównym celem programu „Apollo” jest stworzenie pierwszego polskiego, całkowicie biodegradowalnego, uwalniającego lek stentu do naczyń wieńcowych o cienkim profilu przęsła. Stent taki zachowuje się w sposób bardziej naturalny i goi się lepiej niż dostępne obecnie na rynku stenty o grubym profilu przęsła, przez co jest znacznie lepiej tolerowany przez żywy organizm.
- Nasz stent jest tzw. kopolimerem, co nadaje mu większą wytrzymałość i dzięki temu może być nieco cieńszy. Naturalnie się rozszerza i jest bardziej elastyczny niż stenty metaliczne, a proces jego wchłaniania do organizmu jest bardziej kontrolowany. Po około 2 latach, po spełnieniu zadania jakim jest udrożnienie naczynia i uwolnienie leku, nie pozostawi żadnego śladu w ciele pacjenta. Daje to duże nadzieje na minimalizację ryzyka późnych powikłań takich jak zakrzepica czy zawał serca u ludzi – tłumaczy doc. Piotr Buszman, Kierownik Programu „Apollo”, wicedyrektor ds. badań przedklinicznych CBR AHP.
- Prototyp wszczepionego w ramach badań przedklinicznych stentu powstał w rekordowo krótkim czasie zaledwie 9 miesięcy od podpisania umowy konsorcjum. Realizacja grantów w tempie zgodnym z założonym planem wciąż jest rzadkością w polskich realiach. Nam udało się wyprzedzić zakładany harmonogram. Tym bardziej jesteśmy dumni z tego osiągnięcia – mówi doc. Piotr Buszman.
Badania na modelu tętnic wieńcowych świni domowych to pierwszy ważny krok milowy w badaniu, które w kolejnych fazach skupi się na dopracowywaniu architektury stentu, kontrolowalności jego wchłaniania do organizmu i uwalniania leku.
- Jeśli testy w modelu zwierzęcym dadzą pozytywne rezultaty, będzie można zacząć planować badania kliniczne, a po uzyskaniu odpowiedniego certyfikatu, ich seryjną produkcję i wprowadzenie na rynek – mówi doc. Buszman. vNaukowcy chcą, aby po zakończeniu wszystkich badań ten innowacyjny stent był łatwo dostępny nie tylko dla chorych w Polsce, ale również za granicą.
- Zaletą naszego polskiego stentu będzie jego przystępna cena. Na światowym rynku medycznym dostępne są obecnie tylko trzy tego typu wyroby medyczne, których koszt mieści się w granicach od 2 do 3,5 tys. zł za sztukę. Są one więc mało dostępne dla pacjentów – mówi doc. Krzysztof Milewski, Koordynator Programu „Apollo”, dyrektor generalny CBR AHP. Do tej pory udawało nam się tworzyć i wprowadzać na rynek wyroby znacznie tańsze od tych dostępnych w Europie czy USA. Z wielu z nich z powodzeniem korzystają już nasi koledzy w Unii Europejskiej, Ameryki Południowej, Afryki czy Azji. Mamy nadzieję, że tak będzie i tym razem – dodaje.